de calciu și acizi anorganici, cum ar fi, de exemplu, acidul azotic, acidul clorhidric sau acidul sulfuric. Mai jos este reacția chimică care implică utilizarea acestui ultim acid:
Ca3 (PO4) 2 + 3 H2SO4 → 3 CaSO4 + 2 H3PO4
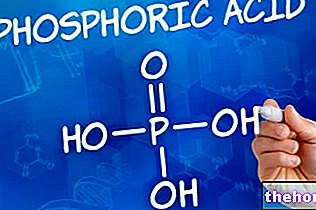
Procesul termic, pe de altă parte, implică obținerea de anhidridă fosforică pornind de la fosforul elementar. Odată formată, anhidrida trebuie apoi hidratată până se obține acidul ortofosforic, așa cum se ilustrează în următoarea reacție:
P2O5 + 3 H2O → 2 H3PO4
Acest ultim proces dă naștere în general unui acid ortofosforic mai pur decât procesul umed.
din mediu, apare ca un solid alb care se topește la o temperatură de aproximativ 42 ° C.
Cu toate acestea, acidul fosforic este comercializat în general sub forma unei soluții apoase concentrate de 85%. Este o soluție incoloră, inodoră și non-volatilă, dar corozivă și cu o consistență destul de densă, aproape „siropoasă”.
Pe lângă faptul că este solubil în apă, acidul ortofosforic este, de asemenea, solubil în etanol, nu este nici exploziv, nici inflamabil, dar datorită corozivității sale asupra pielii și mucoaselor, trebuie totuși manipulat cu mare atenție.
pentru a favoriza aderența materialelor de cimentare pentru capsule, punți, fațete, umpluturi etc. În acest context, acidul ortofosforic este utilizat în general în soluții de 37%.













.jpg)








