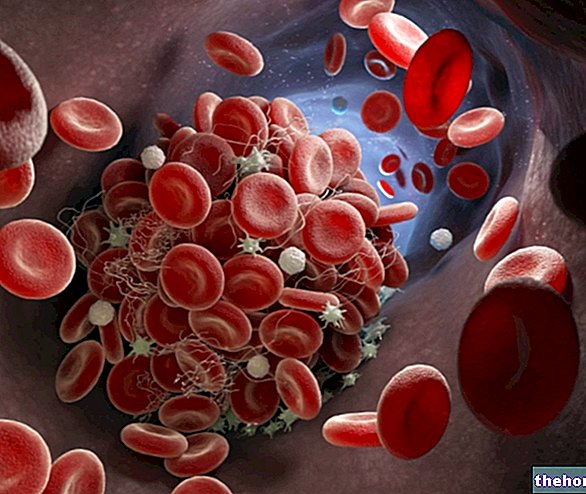
2,3 difosfoglicerat (2,3 DPG) este un compus derivat dintr-un produs intermediar al glicolizei; este concentrat în special la nivelul eritrocitelor, deoarece celulele roșii din sânge - fiind lipsite de mitocondrii - exploatează metabolismul lactacid anaerob (fermentarea homolactică a glucozei) pentru a obține energie.

Hemoglobina este o proteină tetramerică, care este alcătuită din patru subunități, două alfa și două beta, fiecare alcătuită dintr-o porțiune de proteină (globină) și un hem (grup protetic care leagă oxigenul). 2,3-difosfogliceratul se atașează de lanțurile beta, compactându-le și reducând afinitatea hemoglobinei pentru oxigen.
Legarea 2,3 DPG de hemoglobină are loc atunci când este în formă dezoxigenată, în timp ce este dizolvată în plămâni prin legarea hemoglobinei cu oxigenul. De fapt, atunci când hemoglobina ajunge la țesuturi, lanțurile β sunt primii care eliberează oxigenul și această pierdere implică o deplasare a monomerilor din centru. De îndată ce cavitatea hidrofilă internă se deschide, DPG intră și se leagă de tetramer formând legături heteropolare între grupurile sale încărcate negativ și lizină și histidină reziduurile lanțurilor Beta, încărcate pozitiv. Structura stabilizată poate elibera și oxigenul celor două lanțuri α. În plămâni, însă, are loc procesul invers; la presiune ridicată de oxigen, lanțurile α sunt primele care îl leagă și DPG-ul este „stors” și expulzat din tetramer, permițând o legătură mai ușoară a lanțului Oxigen-β.
Bifosfogliceratul 2,3 nu se poate lega de hemoglobina fetală, deoarece această moleculă este lipsită de lanțurile B cu care se leagă 2,3 DPG. Aceasta explică afinitatea mai mare pentru oxigenul hemoglobinei fetale decât hemoglobina maternă, caracteristică care permite sângelui fetal extrage oxigen din sângele matern.