Ingrediente active: mesilat de gabezat
FOY 100 mg pulbere și solvent pentru soluție perfuzabilă
Indicații De ce se folosește Foy? Pentru ce este?
CATEGORIA FARMACOTERAPEUTICĂ
Mesilatul de gabezat aparține categoriei SERPIN, adică inhibitori ai serinei proteazei, substanțe produse în diferite părți ale corpului. Este un medicament sintetic (de natură neproteică) și cu greutate moleculară mică, cu un efect inhibitor ridicat împotriva calikreinei, tripsina, precum și o puternică acțiune relaxantă asupra sfincterului Oddi.
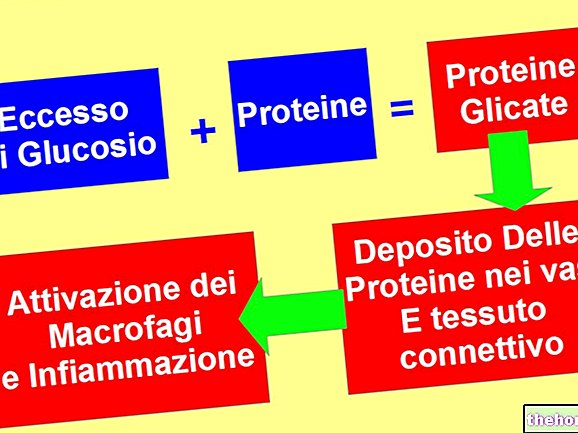
Datorită acestor caracteristici, produsul are un efect pozitiv în rezolvarea simptomelor și corectarea mecanismelor patogenetice ale pancreatitei acute asociate cu eliberarea exagerată sau necontrolată a enzimelor proteolitice.
INDICAȚII TERAPEUTICE
Pancreatita acuta.
Contraindicații Când nu trebuie utilizat Foy
Hipersensibilitate la mesilat de gabesat
Precauții pentru utilizare Ce trebuie să știți înainte să luați Foy
Produsul poate avea o acțiune anticoagulantă.
În unele studii efectuate la câini la doze mari, s-a observat o reducere a timpului parțial de tromboplastină.
Acest eveniment nu a fost observat până în prezent în timpul terapiei Foy la om.
Administrarea acestui produs în doze mari poate provoca ulcere necrotice la locul injectării și de-a lungul vaselor de sânge, unde poate deteriora peretele vascular provocând flebită și rigidizarea vasului în sine.
Pacienții trebuie monitorizați cu atenție.
Dacă apare durere, roșeață sau inflamație la locul injectării, tratamentul trebuie oprit sau locul injectării trebuie modificat și trebuie luate măsurile corespunzătoare.
În timpul administrării pacientul trebuie monitorizat în mod constant.
Pot apărea șoc, șoc anafilactic, reacții anafilactoide.
În caz de scădere a tensiunii arteriale, strângere precordială, dispnee, pierderea cunoștinței, edem faringian / laringian, mâncărime sau stare de rău, tratamentul trebuie oprit imediat și trebuie luate măsurile adecvate.
De asemenea, pacienții trebuie monitorizați îndeaproape pentru apariția posibilă a: agranulocitozei, leucopeniei, trombocitopeniei și hiperkaliemiei.
Dacă se găsesc valori anormale, tratamentul trebuie oprit și, în cazul hiperkaliemiei, trebuie luate măsuri adecvate.
Dacă apar dureri de cap, timp de tromboplastină parțial redus, tendință de sângerare, hipotensiune arterială, greață, vărsături, diaree, erupții cutanate, mâncărime sau congestie facială, doza trebuie redusă. În caz de persistență, suspendați definitiv tratamentul.
Interacțiuni Care medicamente sau alimente pot modifica efectul Foy
Nu se cunosc interacțiuni medicamentoase.
Spuneți medicului dumneavoastră sau farmacistului dacă ați luat recent orice alte medicamente, chiar și cele fără prescripție medicală.
Avertismente Este important să știm că:
A se utiliza dacă sunteți gravidă sau alăptați
. În cazul unei sarcini stabilite sau presupuse, este recomandabil să mențineți doza de Foy la nivelurile minime eficiente și numai pentru indicațiile care implică o viață gravă pentru femeia gravidă.
Pe de altă parte, nu sunt disponibile date despre posibila excreție în laptele matern.
Dozare și metoda de utilizare Cum se utilizează Foy: Doze
Începeți tratamentul cu 1-3 flacoane pe zi (100-300 mg de mesilat de gabesat) prin perfuzie intravenoasă prin picurare la o rată care nu depășește 8 ml / minut și apoi reduceți doza în raport cu îmbunătățirea tabloului clinic. Dacă este necesar, este posibilă creșterea dozei indicate mai sus cu 1-3 flacoane în aceeași zi.
Introduceți solventul special în flaconul care conține pulbere Foy. Soluția astfel obținută trebuie diluată în continuare în 500 ml soluție Ringer sau glucoză 5%.
Soluția astfel preparată trebuie utilizată imediat sau păstrată la frigider (la 3 ° C), unde rămâne stabilă timp de aproximativ 5 zile.
Este recomandabil să administrați soluția prin i.v. lent, ajustând viteza astfel încât să nu depășească 2,5 mg de mesilat de gabesat pe kg de greutate corporală și pe oră.
În cazul terapiei concomitente cu alte medicamente parenterale, mesilatul de gabesat trebuie administrat separat.
Poziția trebuie adaptată corespunzător în funcție de simptomele pacientului.
Utilizare la vârstnici: După o reducere a funcțiilor fiziologice, se recomandă monitorizarea constantă și precauții, cum ar fi reducerea dozei la vârstnici.
Supradozaj Ce trebuie făcut dacă ați luat prea mult Foy
Nu se cunosc simptome de supradozaj.
Efecte secundare Care sunt efectele secundare ale Foy
Dintr-un studiu clinic, efectuat pe aproximativ 4000 de pacienți tratați cu Foy, au apărut diferite reacții adverse; principalele sunt prezentate în tabelul de mai jos, împărțit pe sistem și frecvență:
Respectarea instrucțiunilor din prospect reduce riscul de efecte nedorite.
Este important să informați medicul sau farmacistul cu privire la orice efect nedorit, chiar dacă nu este descris în prospect.
Expirare și reținere
Expirare: vezi data de expirare indicată pe ambalaj.
Data de expirare indicată se referă la produsul ambalat intact, depozitat corect.
AVERTISMENT: nu utilizați medicamentul după data de expirare indicată pe ambalaj.
Medicamentele nu trebuie aruncate pe calea apei uzate sau a reziduurilor menajere. Întrebați farmacistul cum să aruncați medicamentele pe care nu le mai utilizați. Acest lucru va ajuta la protejarea mediului.
Nu lăsați acest medicament la îndemâna și vederea copiilor.
COMPOZIŢIE
Un flacon de pulbere conține: Ingredient activ: 100 mg mesezat de gabesat. O fiolă de solvent conține: apă pentru preparate injectabile.
FORMA FARMACEUTICĂ ȘI CONȚINUTUL
Pulbere și solvent pentru soluție perfuzabilă. "100 mg pulbere și solvent pentru soluție perfuzabilă" 1 flacon + 1 fiolă de solvent 5 ml
Prospect sursă: AIFA (Agenția italiană pentru medicamente). Conținut publicat în ianuarie 2016. Este posibil ca informațiile prezente să nu fie actualizate.
Pentru a avea acces la cea mai actualizată versiune, este recomandabil să accesați site-ul web AIFA (Agenția italiană pentru medicamente). Declinare de responsabilitate și informații utile.
01.0 DENUMIREA PRODUSULUI MEDICAMENTAL
FOY 100 mg pulbere și solvent pentru soluție pentru perfuzie
02.0 COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ
Un flacon de pulbere conține 100 mg de mesilat de gabesat
Pentru lista completă a excipienților, vezi secțiunea 6.1.
03.0 FORMA FARMACEUTICĂ
Pulbere și solvent pentru soluție perfuzabilă
04.0 INFORMAȚII CLINICE
04.1 Indicații terapeutice
Pancreatita acuta.
04.2 Doze și mod de administrare
Începeți tratamentul cu 1-3 flacoane pe zi (100-300 mg de mesilat de gabesat) prin perfuzie intravenoasă prin picurare la o rată care nu depășește 8 ml / minut și apoi reduceți doza în raport cu îmbunătățirea tabloului clinic. Dacă este necesar, este posibilă creșterea dozei indicate mai sus cu 1-3 flacoane în aceeași zi.
Introduceți solventul special în flaconul care conține pulbere Foy. Soluția astfel obținută trebuie diluată în continuare în 500 ml soluție Ringer sau glucoză 5%.
Soluția astfel preparată trebuie utilizată imediat sau păstrată la frigider (la 3 ° C), unde rămâne stabilă timp de aproximativ 5 zile.
Este recomandabil să administrați soluția prin i.v. lent, reglând viteza astfel încât să nu depășească 2,5 mg de mesilat de gabesat pe kg de greutate corporală și pe oră.
Poziția trebuie adaptată corespunzător în funcție de simptomele pacientului.
Utilizare la vârstnici:
După o reducere a funcțiilor fiziologice, se recomandă monitorizarea constantă și precauțiile, cum ar fi reducerea dozei, la vârstnici.
04.3 Contraindicații
Hipersensibilitate la mesilat de gabesat.
04.4 Avertismente speciale și precauții adecvate pentru utilizare
Produsul poate avea o acțiune anticoagulantă.
În unele studii efectuate la câini la doze mari, s-a observat o reducere a timpului parțial de tromboplastină.
Acest eveniment nu a fost observat până în prezent în timpul terapiei Foy la om.
În timpul administrării produsului (vezi și punctul 4.2), se recomandă ajustarea vitezei de perfuzare, astfel încât să nu depășească 2,5 mg / kg pe oră. În cazul terapiei concomitente cu alte medicamente parenterale este necesar să se administreze mesilatul de gabesat separat.
Administrarea acestui produs în doze mari poate provoca ulcere necrotice la locul injectării și de-a lungul vaselor de sânge, unde poate deteriora peretele vascular provocând flebită și rigidizarea vasului în sine.
Pacienții trebuie monitorizați cu atenție.
Dacă apare durere, roșeață sau inflamație la locul injectării, tratamentul trebuie oprit sau locul injectării trebuie modificat și trebuie luate măsurile corespunzătoare.
În timpul administrării pacientul trebuie monitorizat în mod constant. Pot apărea șoc, șoc anafilactic, reacții anafilactoide.
În caz de scădere a tensiunii arteriale, strângere precordială, dispnee, pierderea cunoștinței, edem faringian / laringian, mâncărime sau stare de rău, tratamentul trebuie oprit imediat și trebuie luate măsurile adecvate.
De asemenea, pacienții trebuie monitorizați îndeaproape pentru apariția posibilă a: agranulocitozei, leucopeniei, trombocitopeniei și hiperkaliemiei.
Dacă se găsesc valori anormale, tratamentul trebuie oprit și, în cazul hiperkaliemiei, trebuie luate măsuri adecvate.
Dacă apar dureri de cap, timp de tromboplastină parțial redus, tendință de sângerare, hipotensiune arterială, greață, vărsături, diaree, erupții cutanate, mâncărime sau congestie facială, doza trebuie redusă. În caz de persistență, suspendați definitiv tratamentul.
04.5 Interacțiuni cu alte medicamente și alte forme de interacțiune
Necunoscut.
04.6 Sarcina și alăptarea
Sarcina
În timpul unei sarcini stabilite sau presupuse, este recomandabil să mențineți doza de Foy la nivelurile minime eficiente (a fost observată o pierdere în greutate a fătului la șoareci cu doze de 100 mg / kg / zi) și numai pentru indicațiile care implică viață- amenințând gravida.
Timp de hrănire
Nu sunt disponibile date privind posibila excreție în laptele matern.
04.7 Efecte asupra capacității de a conduce vehicule și de a folosi utilaje
Nu este relevant deoarece Foy este administrat doar într-un spital.
04.8 Efecte nedorite
Dintr-un studiu clinic, efectuat pe aproximativ 4000 de pacienți tratați cu Foy, au apărut diferite reacții adverse; principalele sunt prezentate în tabelul de mai jos, împărțit pe sistem și frecvență:
Raportarea reacțiilor adverse suspectate.
Raportarea reacțiilor adverse suspectate care apar după autorizarea medicamentului este importantă, deoarece permite monitorizarea continuă a raportului beneficiu / risc al medicamentului. Profesioniștii din domeniul sănătății sunt rugați să raporteze orice reacții adverse suspectate prin intermediul sistemului național de raportare. "Adresa https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Supradozaj
Nu se cunosc simptome de supradozaj.
05.0 PROPRIETĂȚI FARMACOLOGICE
05.1 Proprietăți farmacodinamice
Grupa farmacoterapeutică: antihemoragice, antifibrinolitice, inhibitori de protează
- codul ATC: B02AB
Mesilatul de gabezat (GM) s-a dovedit a fi deosebit de activ ca inhibitor al tripsinei, fosfolipazei A, plasminei, calicreinei și trombinei (chiar și în absența AT III), interferând favorabil cu hiperproteazemia pancreatică, fibrinoliza, coagularea și chinina. proprietăți antiplachetare, exercită un efect protector asupra pancreatitei acute induse experimental la șobolani și iepuri, un efect inhibitor asupra DIC indusă la iepuri, șobolani și câini, o acțiune protectoare în diferite tipuri de șoc. Mai mult, la câine, ar putea fi demonstrată o acțiune evidentă de eliberare a sfincterului lui Oddi.
05.2 "Proprietăți farmacocinetice
Timpul de înjumătățire plasmatică al GM este de aproximativ 60 de secunde. Administrat iv la subiecți bărbați sănătoși la o rată de 2 mg / kg / h atinge concentrația maximă în 5-10 minute de la începutul administrării cu un nivel sanguin de principiu activ nemetabolizat egal cu 109 ng / ml. La doza de 4 mg / kg / h, nivelul sanguin al produsului nemetabolizat este egal cu 265 ng / ml.
După administrarea intravenoasă, acesta este metabolizat rapid în acid guanidinocaproic și parabenzoat (ambii inactivi). Eliminarea are loc peste 24 de ore în principal în urină, cu o excreție biliară minimă.
05.3 Date preclinice de siguranță
Studiile de toxicitate acută au arătat valori ale LD50 (mg / kg) variind de la 8000 la 260 mg / kg și de la 7770 la 81 mg / kg la șoareci și șobolani, respectiv dacă sunt administrate oral sau intravenos.
GM este tolerat în mod satisfăcător pentru administrarea repetată la diferite specii de animale.
La șobolani, doza de 40 mg / 5 ml / kg a prezentat mortalitate în proporție de 4/10 / sex, rigiditate a extremităților, inhibarea respirației, reducerea hemoglobinei, hematocritului și timpului de protrombină. La iepuri, tratamentul timp de 6 luni, la doze de 10, 20, 40, 80 și 160 mg / kg / zi administrat intravenos, nu a produs niciun efect, cu excepția unei ușoare iritații locale la locurile de inoculare. La câini, tratamentul cu 40 mg / kg / zi timp de 14 zile a dus la o reducere semnificativă a timpului parțial de tromboplastină, la creșterea greutății ficatului cu degenerare ușoară prin hidropizie. Doza de 640 mg / kg / zi a cauzat, de asemenea, o scădere a hematocritului și a trombocitelor și o creștere a fosfatazei alcaline și a alaninei aminotransferazei.
Datele privind toxicitatea fetală au demonstrat că efectele netoxice la mamă și la produsul de concepție au fost de 50 mg / kg, 20 mg / kg și 10 mg / kg la șoareci, șobolani și iepuri, respectiv. Produsul nu produce efecte asupra fertilității și capacității de reproducere la doze maxime cuprinse între 12 și 36 mg / kg.
Mai mult, compusul nu produce efecte mutagene, după cum arată studiile efectuate pe diferite sisteme genetice.
06.0 INFORMAȚII FARMACEUTICE
06.1 Excipienți
Fiolă cu solvent: apă pentru preparate injectabile
06.2 Incompatibilitate
În cazul terapiei concomitente cu alte medicamente parenterale este necesar să se administreze mesilatul de gabesat separat.
06.3 Perioada de valabilitate
3 ani.
Soluția reconstituită, preparată prin adăugarea conținutului flaconului de solvent corespunzător într-un flacon, este stabilă pentru o perioadă de 24 de ore la temperatura camerei și timp de 5 zile la frigider (3 ° C).
06.4 Precauții speciale pentru depozitare
Nici unul
06.5 Natura ambalajului imediat și conținutul ambalajului
Flacon cu pulbere
Flacon din sticlă neutră incoloră de tip I cu dop din cauciuc butilic și capac din aluminiu / plastic tip „Flip-off”.
Flacon cu solvent
Flacon din sticlă neutră de tip I, incolor.
"100 mg pulbere și solvent pentru soluție perfuzabilă" 1 flacon + 1 fiolă de solvent 5 ml
06.6 Instrucțiuni de utilizare și manipulare
A se vedea secțiunea 4.2.
07.0 DEȚINĂTORUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
Sanofi S.p.A. - Viale L. Bodio, 37 / B - Milano
08.0 NUMĂRUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
A.I.C. n. 026829010 - "100 mg pulbere și solvent pentru soluție perfuzabilă" 1 flacon + 1 fiolă de solvent 5 ml
09.0 DATA PRIMEI AUTORIZAȚII SAU REÎNNOIREA AUTORIZAȚIEI
Data primei autorizații: 28.04.1993
Data celei mai recente reînnoiri: 19.05.2008